Нобелівську премію з фізіології та медицини вручили за революційне відкриття в терапії раку
Нобелівську премію з фізіології та медицини у 2018 році вручили за "відкриття терапії при ракових захворюваннях, яке полягає у гальмуванні негативного імунного регулювання".
Це оголосили на прес-конференції Нобеліського комітету у понеділок, 1 жовтня.
Нагороджені за це спільно Джеймс П. Еллісон та Тасуку Хончо.
BREAKING NEWS
— The Nobel Prize (@NobelPrize) 1 октября 2018 г.
The 2018 #NobelPrize in Physiology or Medicine has been awarded jointly to James P. Allison and Tasuku Honjo “for their discovery of cancer therapy by inhibition of negative immune regulation.” pic.twitter.com/gk69W1ZLNI
Відкриття, зроблене двома лауреатами медицини, використовує здатність імунної системи атакувати ракові клітини, знімаючи з гальм імунні клітини.
This year’s #NobelPrize constitutes a landmark in our fight against cancer. The discovery made by the two Medicine Laureates takes advantage of the immune system’s ability to attack cancer cells by releasing the brakes on immune cells. pic.twitter.com/2mppP3NT19
— The Nobel Prize (@NobelPrize) 1 октября 2018 г.
Джеймс П. Еллісон вивчав білок і виявив, що він діє як гальмо на імунну систему.
Вчений зрозумів, що цей гальмівний потенціал можна використовувати для того, щоб організм атакував пухлину.
Він втілив цю концепцію у новому підході для лікування пацієнтів.
У свою чергу Тасуку Хонджо, також нагороджений премією, виявив, що імунні клітини також гальмує протеїн, але має інший механізм дії.
Терапія, яку розробили на основі його відкриття, виявилася вражаюче ефективною у боротьбі з раком.
Cancer kills millions of people every year and is one of humanity’s greatest health challenges. By stimulating the ability of our immune system to attack tumour cells, this year’s #NobelPrize laureates have established an entirely new principle for cancer therapy. pic.twitter.com/6HJWsXw4bE
— The Nobel Prize (@NobelPrize) 1 октября 2018 г.
Рак кожен рік вбиває мільйони людей і є однією з найбільших проблем у галузі здоров'я. Стимулюючи здатність нашої імунної системи атакувати пухлинні клітини, цьогорічні лауреати Нобелівської премії "знайшли зовсім новий принцип лікування раку".
До відкриттів, які змогли зробити Еллісон та Хонджо, прогрес у клінічному розвитку був скромним.
"Імунна контрольна топотерапія" зробила революцію в лікуванні раку і кардинально змінила спосіб, у який можна керувати раком", – зазначають у Нобелівському комітеті.
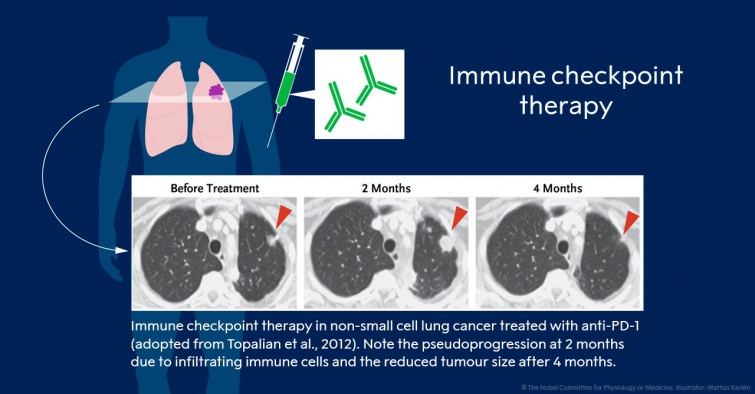 |
| "Імунна контрольна топотерапія" зробила революцію в лікуванні раку |
Джеймс П. Еллісон народився у 1948 році в Техасі, США. Він професор MD Anderson Cancer Center Університету штату Техас, а також співпрацює з Інститутом Паркера з онкологічної імунотерапії.
Тасуку Хонджо народився у Японії у 1942 році, з 1984 року він є професором Університету Кіото.
Just in! Nobel Laureate Tasuku Honjo, surrounded by his team at Kyoto University, immediately after hearing the news that he had been awarded the 2018 #NobelPrize in Physiology or Medicine. pic.twitter.com/8TdlnXiSLe
— The Nobel Prize (@NobelPrize) 1 октября 2018 г.
ЧИ МОЖЕ НАША ІМУННА СИСТЕМА ЗАХИЩАТИСЬ ВІД РАКУ?
Рак включає в себе безліч різних захворювань, усіх їх характеризує неконтрольоване розмноження хворих клітин, здатних поширюватися на здорові органи та тканини.
Існує ряд терапевтичних підходів для лікування раку, включаючи операції, радіацію та інші стратегії, деякі з яких отримали попередні Нобелівські премії.
Зокрема, Нобеля давали за лікування гормонами раку передміхурової залози (Хаггінс, 1966), хіміотерапію (Elion and Hitchins, 1988) і трансплантацію кісткового мозку при лейкемії (Thomas 1990).
Однак рак досі залишається надзвичайно важким для лікування.
В кінці 19 ст і початку 20 ст виникла концепція, що активація імунної системи може бути стратегією атаки на клітини пухлин клітин. Тоді спробували інфікувати пацієнтів бактеріями, щоб активувати захист. Ці зусилля мали скромні результати, однак варіант цієї стратегії використовують сьогодні при лікуванні раку сечового міхура.
Зрозуміло, що потрібні були знання. Ряд учених займалися інтенсивним фундаментальним дослідженням та розкрили фундаментальні механізми, що регулюють імунітет, а також показали, як імунна система може розпізнавати ракові клітини.
Незважаючи на значний науковий прогрес, спроби розробити загальні нові стратегії проти раку виявилися складними.
ПРИСКОРЮВАЧІ ТА ГАЛЬМА В НАШІЙ ІМУННІЙ СИСТЕМІ
Фундаментальною властивістю нашої імунної системи є здатність захищатися від бактерій, вірусів та інших небезпек.
Т-клітини, тип білих кров'яних тілець, є ключовими гравцями в цій обороні.
Т-клітини мають рецептори. Саме за допомогою них вони взаємодіють з іншими клітинами, і це спонукає імунну систему зайнятися захистом.
Але додаткові білки, що діють як Т-клітинні прискорювачі, також необхідні для запуску повноцінної імунної відповіді.
Багато вчених сприяли цьому важливому фундаментальному дослідженню та визначили інші білки, які гальмують Т-клітини, пригнічуючи імунну активацію.
Цей складний баланс між прискорювачами та гальмами необхідний для жорсткого контролю. Це гарантує, що імунна система достатньо займатиметься атакою на чужорідні мікроорганізми, уникаючи надмірної активації, яка може призвести до аутоімунного руйнування здорових клітин і тканин.
НОВИЙ ПРИНЦИП ДЛЯ ІМУННОЇ ТЕРАПІЇ
У 1990-х роках у своїй лабораторії в Каліфорнійському університеті Берклі Джеймс П. Елісон вивчав Т-клітинний білок CTLA-4. Він був одним з декількох вчених, які зробили спостереження, що CTLA-4 гальмує Т-клітини.
Еллісон розробив антитіло, яке може зв'язуватися з CTLA-4 і блокувати його функцію (див. малюнок).
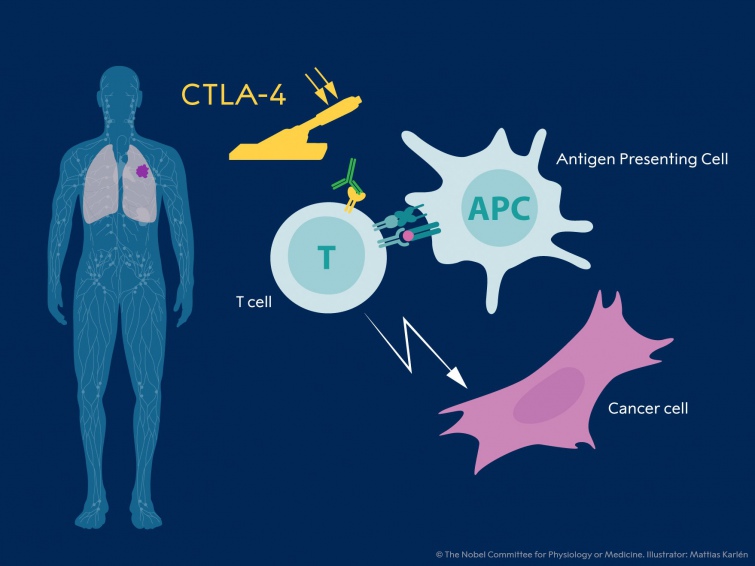 |
| Джеймс П. Еллісон вивчав білок, і виявив, що він діє як гальмо на імунну систему |
Перший експеримент він та його співробітники провели у 1994 році. Результати були вражаючими: миші з раком виліковувались антитілами, які блокують гальмо і розпалюють протипухлинну Т-клітину.
Незважаючи на незначний інтерес фармацевтичної галузі, Еллісон продовжував активні зусилля по розробці стратегії в терапії для людей. Перспективні результати незабаром з'явилися у кількох груп, а в 2010 році важливе клінічне дослідження показало вражаючі ефекти у пацієнтів з меланомою, типом раку шкіри.
У декількох пацієнтів зникли ознаки залишкового раку. Таких чудових результатів ніколи раніше не було в цій групі пацієнтів.
ВІДКРИТТЯ PD-1 ТА ЙОГО ЗНАЧЕННЯ ДЛЯ ЛІКУВАННЯ РАКУ
У 1992 році, за кілька років до відкриття Еллісона, Тасуку Хонджо відкрив PD-1, інший білок, який виражений на поверхні Т-клітин.
У своїй лабораторії в Кіотоському університеті він провів багато років і виявив, що PD-1, подібний до CTLA-4, гальмує Т-клітини, але працює за іншим механізмом (див. малюнок).
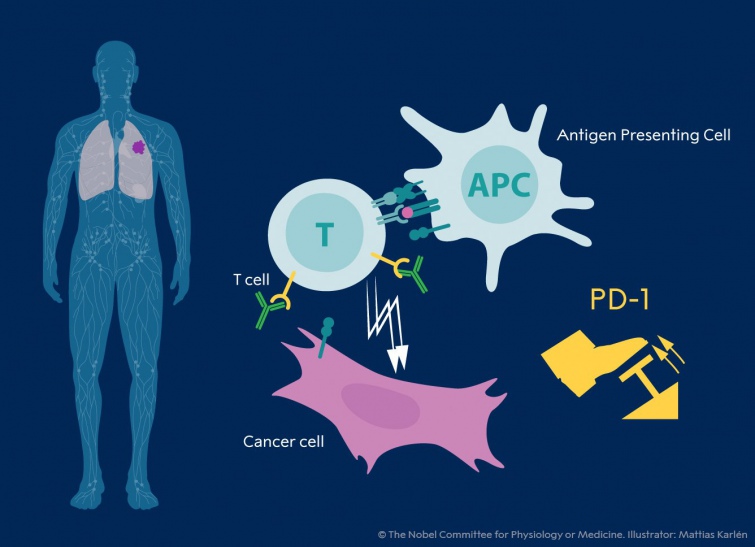 |
| Тасуку Хонджо, також нагороджений премією, виявив, що гальмує імунні клітини протеїн |
В експериментах на тваринах Хонджо також виявив, що блокада PD-1 є перспективною стратегією боротьби з раком.
Клінічні дослідження тривали до 2012 року, коли ключове з них чітко продемонструвало ефективну терапію пацієнтів з різними типами раку.
У деяких хворих це була тривала ремісія, а у декількох пацієнтів з метастатичним раком, стан яких раніше вважали невиліковним, з`явилися перспективи лікування.
ІМУННА КЛІНІЧНА ТЕРАПІЯ ДЛЯ РАКУ СЬОГОДНІ І В МАЙБУТНЬОМУ
Після первинних досліджень, що показали наслідки блокади CTLA-4 та PD-1, науковці почали практикувати лікування, яке часто називають "імунною контрольно-пропускною терапією".
Воно принципово змінило результати для певних груп хворих на рак.
[L]Однак таке лікування має несприятливі побічні ефекти, які можуть бути серйозними та навіть загрожувати життю. Вони зумовлені надмірною реакцією імунної системи, що веде до аутоімунних реакцій.
Інтенсивне продовження досліджень наразі орієнтоване на з'ясування механізмів дії блокади CTLA-4 та PD-1 з метою поліпшення терапії та зменшення побічних ефектів.
З двох стратегій лікування, контрольно-пропускна терапія проти PD-1 виявилася більш ефективною і позитивні результати спостерігаються при таких типах захворювання, як рак легенів, рак нирок, лімфома та меланома.
Нові клінічні дослідження вказують на те, що комбінована терапія, орієнтована як на CTLA-4, так і на PD-1, може бути ще більш ефективною, як це продемонстровано у пацієнтів з меланомою.
Наразі тривають ряд пробних терапевтичних випробувань проти більшості видів раку.