Дихайте повільніше: що варто знати про Нобелівську премію з медицини 2019

Гіпоксія або нестача кисню.
Що вам перше спадає на думку, коли ви чуєте цей термін?
Напевно, щось дуже неприємне, як наприклад, смерть чи хвороба.
Гіпоксія дійсно може супроводжувати такі захворювання як інфаркт, інсульт, інфекції або анемія. А ще цей стан виникає у людини, яка певний проміжок часу перебуває під водою, затримуючи дихання.
Проте гіпоксія – не завжди патологічний процес. Наш організм весь час пристосовується до різних рівнів кисню. І цього року, Нобелівську премію з медицини та фізіології вчені отримали за дослідження того, як "клітини відчувають доступність кисню та адаптуються до неї".
Премію розділили між собою американці Вільям Кейлін молодший та Грегг Семенза, а також британець Пітер Редкліфф.
За що ж вручили цьогорічного Нобеля з медицини пояснюємо за допомогою українських науковців:
- Тетяни Древицької, к.б.н., старшого наукового співробітника Інституту фізіології ім. О.О.Богомольця НАН України;
- Віктора Досенка, завідувача відділом загальної та молекулярної патофізіології Інституту фізіології НАН України.
За що саме вручили Нобеля
Коли в організмі починається гіпоксія, то організм виділяє велику кількість гормону еритропоетину, який підвищує виробництво червоних кров'яних тілець (еритроцитів).
Як саме на цей гормональний процес впливає кисень довгий час було загадкою.
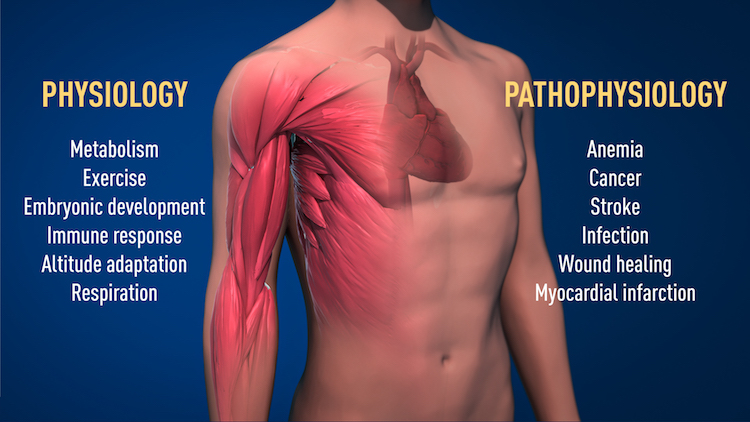 |
| Патологія та фізіологія гіпоксії. Фото: Nobel Prize |
Лише нещодавно науковці змогли ідентифікувати молекулярно-генетичні механізми, які регулюють активність генів, що відповідають на зміни у рівні кисню.
Вчені проводили дослідження на генетично-модифікованих мишах. Вони вивчали їхні гени, які відповідають за відповідь на гіпоксію, і виявилось, що ділянки ДНК, розташовані поряд з цими генами, виступають у ролі медіаторів.
А у дослідах на культурованних клітинах печінки знайшли протеїновий комплекс, який зв'язується з цими ДНК-ділянками і залежить від кисню.
Цей протеїновий комплекс вони назвали фактором, що індукується гіпоксією або просто HIF.
HIF – це специфічний протеїн, що зв'язується з ДНК та бере участь у підтримці гомеостазу, тобто процесі існування та функціонування клітини.
[BANNER1]
"Процеси адаптації та чутливості організму до рівня кисню вже оточені Нобелівськими преміями.
Ще у 1931 році Отто Варбур отримав Нобелівську премію за відкриття природи та функції дихальних ферментів мітохондрій.
В цьому ж десятиріччі (1938 рік) премію дали Корнею Хеймансу за з'ясування механізмів чутливість до коливань кисню на рівні організму, наука зрозуміла, де знаходяться рецептори, як вони працюють, як впливають на дихання та серцево-судинну систему", – розповідає Тетяна Древицька, к.б.н., старший науковий співробітник Інституту фізіології ім. О.О.Богомольця НАН України.
І Редкліф, і Клейн, і Семенца, вивчали дію еритропоетину на організм.
 |
| Лауреати Нобелівської премії з фізіології та медицини 2019 |
Донедавна найбільшим питанням було те, що в нашому організмі найпершим реагує на зниження рівню кисню в організмі.
"Тут була купа кандидатів. Науковці знайшли велику кількість киснезалежних ферментів. Але на цьому все зупинялося. Всі знахідки були обрубані.
Білок HIF, який винайшов Семенца, і став тим ключиком, який зміг пояснити всі ці важливі адаптаційні механізми", – каже завідувач відділом загальної та молекулярної патофізіології Інституту фізіології НАН України Віктор Досенко.
У стані гіпоксії всіх інших білків стає менше, а кількість HIF збільшується. Цьому сприяє нестача кисню.
І механізм цей є універсальний. Він присутній в усіх клітинах і знайдений у всіх тварин.
 |
Як працюють білки HIF у нашому організмі
Існує четверо "братів" HIF: HIF 1-альфа, HIF 1-бета, HIF 2-альфа, HIF 3-альфа.
Всі брати активуються при нестачі кисню.
Природа подбала про те, що якщо один член цієї родини не спрацює, то його функції візьме на себе інший.
"Важливо розуміти, що HIF руйнується. Він виділяється, живе не довгим, приблизно, 5-хвилинним життям та зникає", – зауважує Тетяна Древицька.
Як він руйнується? Його "мітить" спеціальний фермент, який називається HIF-пролілгідроксилаза. Це молекула, яка чутлива до кисню, і вона приєднує до білка гідроксид, що запускає процес руйнування HIF.
"Це дуже ресурсозатратний процес, – зазначає Віктор Досенко. – Виробити білок важко і руйнувати його весь час може здатись безглуздим з точки зору логіки. Але кисень настільки важливий для нас, що цей адаптаційний процес має сенс попри всі зусилля.
У стані гіпоксії білок HIF має можливість не руйнуватись, а накопичуватись, це дає нам, в разі зниження кисню, – адаптуватись і вижити".
 |
У родині братів HIF є "дивак" – третя ізоформа HIF (HIF 3-альфа), чия функція буквально – це заважати іншим HIF-білкам забезпечувати адаптацію до гіпоксії.
"Дивак" він в генетичному плані: він може впізнавати гени-мішені, але позбавлений можливості їх вмикати.
"Адаптація до гіпоксії має бути дозованою і третя ізоформа HIF гальмує роботу інших братів. Він бачить ген, але не вмикає, а ніби затуляє собою, щоб не дати "братам" його розгледіти", – пояснює науковець.
В Інституті фізіології НАН України проводили дослід, щоб зрозуміти, що буде якщо вимкнути цей гальмівний процес.
"Ми проводили дослідження на щурах, тренували тварин плавати. Вимикали ген HIF 3-альфа і щури без цього гену плавали на 40% краще", – розповідає Тетяна Древицька.
Але після експерименту м’язи щурів були дуже пошкоджені. Тканини не витримали відсутності молекулярного гальма.
Накопичення та активна робота трьох форм HIF дозволило щурам діяти на межі можливостей, завдяки тому, що протеїни покращили роботу м’язів.
[BANNER2]
Ось ще один приклад, який допоможе оцінити важливість цих гальмівних процесів.
Завдяки цьому "братику" HIF 3-альфа ви не прокидаєтеся з кровавими очима.
Чому?
У нашої рогівки немає судин. Вона отримує кисень прямо з повітря, поки вдень наші очі розплющені.
Але коли ми спимо, кисню треба подолати багато перепон, щоб дістатися рогівки. Це також стан гіпоксії, і якщо не гальмувати роботу білків, то людина зранку буде прокидатись буквально з кривавими очима.
В чому практичність відкриття
Наш організм весь час відчуває гіпоксію. Наприклад, під час фізичних навантажень.
"І це супер класно! Бо це корисно", – каже Тетяна Древицька.
HIF – основна молекула гіпоксії – бере участь в купі фізіологічних реакцій. Але в розвитку ряду патологій він також бере участь – активується при запаленні, при розвитку пухлин, при інфаркті та інсульті.
"Під час фізичних навантажень він позитивно впливає на наші м’язи, на наш мозок, а от при пухлинному рості – допомагає вже її виживанню та росту", – пояснює науковиця.
І ось тут виникає основна дилема вчених, щодо практичного застосування знань: HIF потрібен всім клітинам і ми не можемо блокувати його, щоб "перекрити" кисень онкологічному утворенню.
"А як бути з клітинами серця, клітинами мозку, клітинами м'язів – вони не виживуть без HIF", – зауважує Віктор Досенко.
Надалі вчені планують дослідити роль HIF 3-альфа у деяких патологічних станах, таких як інфаркт, астма тощо. Для того, щоб запропонувати нові терапевтичні підходи.
Можливо, якщо штучно та точково створити відсутність гальмування відповіді на гіпоксію у певній тканині та органі – це допоможе наситити їх білком HIF та розв'язати певну медичну проблему.
Деякі речі були впроваджені для терапії раку ще до вручення Нобелівської премії.
Наприклад, існує препарат, який заважає формуванню нових кровоносних судин, які можуть підживлювати пухлину.
Препарат містить антитіла проти фактора росту ендотелію судин або VEGF.
І цей фактор VEGF знаходиться під контролем HIF.
Україна та київська школа гіпоксії
В нашій країні існує українська школа гіпоксії.
"Нам є чим пишатися, коли мова йде про вивчення чутливості організму до рівнів кисню.
Є багато речей, які вперше винайшли саме у нас. Вивчення гіпоксії в Україні – це перш за все школа академіка Сиротиніна, який одним з перших зацікавився проблемами гіпоксії та припустив, що цей процес може і лікувати", – пояснює Віктор Досенко.
Патофізіолог Микола Сиротинін – учень Олександра Богомольця і свої дослідження обґрунтовував аномально довгим життям у тих, хто проживає в горах.
 |
| Науковці Віктор Досенко, Тетяна Древицька та патофізіолог Микола Сиротинін |
При Ельбрусі він заснував українську медико-біологічну станцію з вивчення гіпоксії, яка існує й досі.
Там в умовах постійної гіпоксії проживає багато експериментальних тварин.
На основі цих досліджень потім з'явилося те, що визнає весь світ – київська класифікація гіпоксії.
Ці роботи були базою для створення спеціального методу – інтервальної гіпоксії й перших приладів для її відтворення.
Перший космонавт України Леонід Каденюк проходив підготовку на апаратах з гіпоксичних тренувань, які відтворювали гірські умови.
"У нас, в Інституті фізіології, є відділ з вивчення проблем гіпоксії, який спеціалізовано займається цими проблемами, – розповідає Тетяна Древицька.
Довгий час цим відділом завідувала Ірина Микитівна Маньковська. Під її керівництвом і розпочалося вивчення молекулярно-генетичних механізмів відповідей на гіпоксію – HIF, VEGF та проліл-гідроксилаз.
Під редакцією Тетяни Серебровської вийшло дві книжки і співавтором цих книжок є і Грегг Семенца", – розповідають науковці.
[BANNER3]
Співавторами однієї з українських книжок про Intermittent hypoxia, що можна перекласти як "переривчаста гіпоксія" разом із лауреатом Нобелівської премії, стали і консультанти нашої статті – Віктор Досенко та Тетяна Древицька.
Але попереду ще багато питань і багато досліджень.
Тож, дихаймо повільніше, періодично, затримуємо повітря!
Наталія Бушковська, УП.Життя
Титульні світлини від Depositphotos
Вас також може зацікавити:
Назвали лауреатів Нобелівської премії з хімії 2019. Що вони відкрили
Назвали лауреатів Нобелівської премії з фізики 2019. Що вони відкрили
Ми хочемо тримати з вами зв'язок. Будемо раді бачитися і спілкуватися з вами на нашій сторінці у Facebook.
А якщо хочете бути в курсі лише новин та важливої інформації про здоров'я, підписуйтесь на нашу Facebook-групу про здоров'я та здоровий спосіб життя.